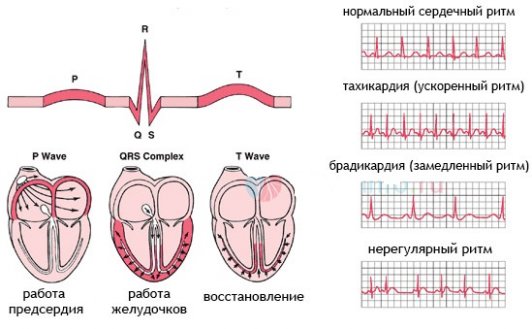
Брадикардия: понятие, виды
Содержание
Брадикардия — это типовая форма нарушения деятельности сердца кардиогенного и внесердечного происхождения, характеризующаяся уменьшением частоты сокращений сердца (менее 60 уд. в 1 мин). Различают физиологическую и патологическую формы брадикардии. Брадикардия – замедленное сокращения сердца до частоты менее 60 ударов в минуту у взрослых. Частота сердечных сокращений зависит от возраста и физического состояния. Сердечный ритм может снижаться ниже 60 уд / мин в норме, например во время глубокого сна – это физиологическая брадикардия.
Более подвержены брадикардии пожилые люди.
Давайте рассмотрим основные причины брадикардии:
1) Нарушения функционирования синусового узлом;
2) Патология проводящих путей сердца (электрические импульсы не проводятся из предсердий в желудочки);
3) Метаболические нарушения, вызванные например гипотермией (пониженной температурой тела);
4) Повреждение сердца в результате инфаркта или других болезней сердца
Симптомы брадикардии:
Замедления ритма сердца, в первую очередь приводит к нарушению кровоснабжения головного мозга с такими симптомами, как: усталость, головокружение, обморок или предобморочные состояния.
Осложнения брадикардии:
Тяжелая и длительная брадикардия может привести к сердечной недостаточности, обморокам (потеря сознания), стенокардии (боль в груди), повышению кровяное давление.
Брадикардия требует медикаментозного лечения, если она длительная или выраженная (менее 50 ударов в минуту).
При тяжелой и длительной брадикардии устанавливается искусственный водитель ритма, который задает нужную частоту сердечных сокращений.
Физиологическую брадикардию регистрируют, например, во время сна — частота сердечных сокращений уменьшается до 30—40 в 1 мин. Такую брадикардию считают нормальным явлением у здорового человека; ее возникновение обусловлено в основном доминирующим влиянием блуждающего нерва на внутренние органы в ночное время.
Вместе с тем, при выраженной брадикардии любого происхождения возможно нарушение кровоснабжения головного мозга и других органов, что может привести к летальному исходу.
Патогенетическую основу брадикардии составляет аномальное снижение автоматизма синусового узла или блокада проведения импульсов по проводящей системе сердца.
Аномальное снижение автоматизма синусового узла
Причинами аномального формирования импульса в синусовом узле могут быть возрастное фиброзирование СА-узла, его воспаление (например, при коллагеновых сосудистых заболевания или вирусной инфекции), ишемия, нарушения электролитного обмена, гипотиреодные состояния.
Наиболее распространенной причиной дисфункции синусового узла считают применение сердечных препаратов, таких как бета-блокаторы, блокаторы кальциевых каналов, наперстянка, препараты, используемые в психиатрической практике (фенотиазин, литий, амитриптилин) и др. Нередко парасимпатические вегетодистонии характеризуются развитием синусовой брадикардии.
Механизмы аномального снижения автоматизма синусового узла:
1) первичное (абсолютное, по сравнению с нормой) уменьшение автоматической активности СА-узла, позволяющее доминировтать автоматизму замещающих водителей ритма (пейсмекеров II порядка);
2) анормальный автоматизм шпополяризованных специализированных клеток проводящей системы, находящихся за пределами синоатриального узла. В отличие от синусового этот вид автоматизма (например, в волокнах Пуркинье) устойчив к свехчастому подавлению, т.е. после его завершения патологические импульсы возобновляются с прежней частотой. Таким образом, данный тип анормального автоматизма пейсмекеров II порядка становится доминирующим в работе сердца.
Определение местонахождения источника возбуждения
Определение местонахождения источника возбуждения (в т.ч. патологического) – пейсмекера насосной функции сердца осуществляется путем оценки сокращений кардиомиоцитов предсердий и желудочков. При этом необходимо идентифицировать следующие ритмы сократительной функции сердца.
1. Синусовый ритм. Это нормальный ритм сердечной деятельности. Все другие ритмы являются патологическими. Пейсмекером данного ритма является синоатриальный узел. ЭКГ-признаками синусового ритма являются: а) во II стандартном отведении зубцы Р всегда положительные и предшествуют каждому комплексу QRS; б) зубцы Р в одном и том же отведении всегда имеют одинаковую форму.
2. Предсердный ритм. Если источник возбуждения находится в нижних отделах предсердий, то волна возбуждения распространяется на предсердия «снизу вверх» (ретроградно) и поэтому: а) во II и III отведениях зубцы Р отрицательные; б) зубец Р всегда предшествует каждому комплексу QRS.
3. Ритмы из АВ-соединения. При доминировании водителя ритма в атриовентрикулярном (предсердно-желудочковом) узле желудочки возбуждаются как обычно («сверху вниз»), а предсердия — ретроградно (т.е. «снизу вверх»). При данном ритме на ЭКЕ а) зубцы Р могут отсутствовать, т.к. возможно их наслоение на нормальные комплексы QRS; б) зубцы Р могут быть отрицательными и располагаться после комплекса QRS. ЧСС при ритме из АВ-соединения меньше нормы и равна примерно 40—60 уд./мин.
4. Желудочковый ритм (син., идиовентрикулярный ритм; от греч. idios -собственный, и лат. ventriculus — желудочек) развивается в том случае, когда функцию пейсмекера берет на себя проводящая система желудочков. Волна возбуждения распространяется по желудочкам «неправильными» путями и поэтому ее скорость замедлена. Особенности желудочкового ритма: а) комплексы QRS расширены и деформированы (в норме длительность комплекса QRS равна 0,06—0,10 с, а при таком ритме — превышает 0,12 с); б) нет какой-либо закономерности взаиморасположения зубцов Р и комплексов QRS, потому что АВ-соединение не пропускает импульсы из желудочков в предсердия, которые при этом могут возбуждаться как обычно под влиянием нормальной активности синусового узла; в) ЧСС может быть менее 40 уд./мин.
Блокада проведения импульсов по проводящей системе
Блокада проведения импульсов по структурам проводящей системы зависит от нескольких взаимодействующих факторов: силы электрического стимула (потенциала действия) в возбужденном участке волокна, функционального состояния соседнего еще не возбудившегося участка волокна, межклеточного электротонического взаимодействия, пассивных свойств клеточных мембран, гистологических особенностей строения волокон. Изменения каждого из этих факторов могут приводить к нарушениям проводимости.
Нередко причиной медленного проведения или блокады бывает снижение потенциала покоя (максимального диастолического потенциала) в клетках, которым в нормальных условиях свойствен быстрый электрический ответ (клетки Пуркинье, сократительные клетки предсердий и желудочков). Скорость проведения импульса в этих клетках непосредственно связана с крутизной и амплитудой фазы 0 потенциала действия, т. е. с такими характеристиками, которые определяются количеством открытых быстрых Na+-каналов мембраны в момент возбуждения и натриевым электрохимическим градиентом, т. е. соотношением вне- и внутриклеточной концентраций ионов Na+. В свою очередь, существует тесная зависимость между количеством №+-каналов, способных к открытию, и величиной максимального диастолического потенциала мембраны. Если под влиянием патологических воздействий он понижается, то уменьшается потенциал действия и, соответственно, замедляется скорость проведения импульса. Потенциал действия со сниженной фазой 0 за счет инактивации быстрых №+-каналов мембраны характеризует «подавленный быстрый ответ».
При уменьшении потенциала покоя до уровня —50 мВ инактивируется около 50% Ыа+-каналов и возбуждение (проведение импульса) становится невозможным. Возникающие блокады могут быть как однонаправленными, так и двунаправленными.
В части случаев, даже при значительном уменьшении потенциала покоя, проведение импульса может сохраняться, но при этом резко замедляется, детерминируя возникновение брадикардии. Возбуждение клеток, т. е. регенеративная деполяризация мембраны, обеспечивается в этих условиях медленными входящими Са++- и Nа+-токами, поскольку медленные Са++-, Са++/ Na+- и Na+-каналы мембраны устойчивы к снижению потенциала покоя. «Быстрые» клетки превращаются в «медленные» клетки с выраженным уменьшением скорости проведения или с возникновением блокады.
Одной из форм нарушенной проводимости является декрементное (затухающее) проведение, т. е. прогрессирующее замедление проведения импульса в волокне, на протяжении которого постепенно снижается эффективность стимула, т.е. потенциала действия, и/или возбудимость ткани. Этот процесс обычно разворачивается в функционально подавленных волокнах.
Другая форма нарушенной проводимости представлена неравномерным проведением импульса. Если в параллельно расположенных волокнах проведение становится декрементным, но не в одинаковой степени, то вместо единого фронта возбуждения появляются опережающие и запаздывающие волны. В связи с тем что деполяризация соседних волокон происходит неодновременно, общая эффективность стимула падает, и поэтому возможно развитие частичной или полной блокады его проведения.
Многочисленные экспериментальные данные показали, что электротоническое взаимодействие между двумя возбудимыми участками, разделенными небольшой зоной высокого сопротивления, сопровождается резким замедлением проводимости в дистальном участке волокна. Такие факторы, как ограниченная ишемия миокарда, местная высокая концентрация ионов
К+, локальное сдавление или охлаждение и другие воздействия могут вызвать невозбудимость небольшого сегмента в сердечном волокне (напр., в волокне Пуркинье) и тем самым способствовать электротонически опосредованному ступенчатому торможению передачи импульса через невозбудимую зону.
Таковы вкратце особенности механизмов блокирования проведения импульсов. К этому можно добавить, что повторный вход импульса, т.е. механизм re-entry, имеет непосредственное отношение к расстройствам проводимости. Блокировка проводимости, как правило, происходит в области АВ-узла, который электрофизиологически соединяет предсердия и желудочки. В других регионах сердца предсердия и желудочки разделены фиброзными кольцами.
Такая особенность структуры сердца уменьшает вероятность электрической обратной связи между желудочками и предсердиями, но это также означает, что АВ-узел и его пучок особенно уязвимы к факторам, нарушающим проводимость.
Во всех случаях блокада проведения импульсов по проводящей системе выявляется и оценивается по изменению временных параметров (длительности сегментов, интервалов, зубцов) ЭКГ.
Как правило, для оценки проводимости измеряют:
Длительность зубца Р (в норме до 0,1 с) — отражает скорость проведения импульса по предсердиям.
Длительность интервала P—Q /PR/ (интервал Р—Q = длительность зубца Р + сегмент PQ). Длительность данного интервала (в норме 0,12—0,20 с) отражает скорость проведения импульса от предсердий до миокарда желудочков; его увеличение происходит при нарушенном проведении импульсов через предсердно-желудочковый узел, т.е. при атриовентрикулярной блокаде (AV-блокаде).
3 степени AV-блокады
Различают 3 степени AV-блокады:
I степень — интервал P-Q увеличен, но каждому зубцу Р соответствует свой комплекс QRS, т. е. не происходит их выпадения;
II степень — комплексы QRS частично выпадают, т. е. не всем зубцам Р соответствует свой комплекс QRS; также называется Wfenckebach блок.
III степень — полная блокада проведения в АВ-узле. Предсердия и желудочки сокращаются в собственных ритмах, независимо друг от друга, т. е. формируется идиовентрикулярный ритм.
Длительность комплекса QRS (в норме 0,06—0,10 с) — отражает распространение возбуждения по желудочкам.
Длительность т. н. интервала внутреннего отклонения в отведениях Vl и V6. Это время между началом комплекса QRS и зубцом R (норма: в отведении V, до 0,03 с; в отведении V6 до 0,05 с). Этот показатель используют чаще всего для распознавания блокад ножек (ветвей) пучка Гиса и, кроме того, для определения источника возбуждения в желудочках при развитии экстрасистолы (внеочередного сокращения желудочка). В зависимости от того, какая ножка пучка Гиса заблокирована, формируются различные, достаточно характерные паттерны (от англ, pattern — образ) ЭКГ. При полной блокаде правой ветви пучка Гиса прекращается проведение по ней возбуждения к правой половине межжелудочковой перегородки и правому желудочку.
В такой ситуации прежде всего активируется левая ветвь пучка Гиса и, соответственно, левая половина межжелудочковой перегородки и левый желудочек. Затем необычным путем (волна деполяризации поступает по мышечным волокнам от активированного левого желудочка) возбуждается правая половина межжелудочковой перегородки и правый желудочек. Такая необычность распространения волны деполяризации и несогласованность в возбуждениях желудочков находит свое отражение в изменениях комплекса QRS, зарегистрированных в грудных отведениях V, и V6. Таков без деталей, которые не рассматриваются в данном пособии, принципиальный сценарий нарушения работы сердца и ЭКГ при блокаде ножек (ветвей) пучка Гиса.
По уровню поражения проводящей системы выделяют:
1. Синусовую брадикардию, возникающую при нарушении образования импульса в синусовом узле.
2. Брадикардии, возникающие при нарушении проведения импульса из синусового узла по проводящей системе сердца:
— брадикардия при синоатриальной блокаде;
— брадикардия при внутрипредсердной блокаде; брадикардия при атриовентрикулярной блокаде;
— брадикардия при блокаде пучка и ветвей Гиса.
По степени выраженности различают следующие виды брадикардии:
— легкой степени выраженности (ЧСС 50—60 уд./мин);
Щг умеренно выраженную (ЧСС 40—50 уд./мин);
— выраженную брадикардию (ЧСС менее 40 уд./мин).
Брадикардия — это полиэтиологическая форма патологии, которая, как правило, развивается при заболеваниях сердечно-сосудистой системы и их осложнениях (в острой стадии инфаркта миокарда, при кардиосклерозе, ревматических поражениях сердца, миокардитах, кардиомиопатиях и т.д.); поражениях нервной системы (травмы и опухоли головного мозга, нарушения мозгового кровообращения, невротические состояния и др.); эндокринных заболеваниях (гипотиреоз, болезнь Адиссона); передозировке ряда лекарственных препаратов ф-адреноблокаторов, антиаритмических препаратов, блокаторов кальциевых каналов, сердечных гликозидов и др.); инфекционных заболеваниях (брюшной тиф, гепатит, менингококковая инфекция); нарушениях электролитного баланса.
Обычно физиологическую, легкой степени выраженности брадикардию пациенты не ощущают. Симптомы патологической брадикардии определяются заболеванием, на фоне которого произошло урежение сердцебиения. Характерными проявлениями являются: быстрая утомляемость, сонливость, шум в ушах, постоянные головокружения, боли в груди, одышка и др.
Терапия при бессимптомных формах брадикардии и при отсутствии основного заболевания не показана. При умеренной и выраженной брадикардии, сопровождающейся клиническими проявлениями, назначают лечение основного заболевания, при успешном устранении которого брадикардия обычно исчезает. Основным осложнением выраженной брадикардии является синдром Морганьи—Адамса—Стокса (см. ниже).
Синдром слабости синусового узла (СССУ)
Патогенетическую основу СССУ (называемого иногда «болезнь синусового узла») составляет дисфункция (преимущественно, снижение) автоматизма синусового узла, возникающая в условиях его ишемии, дистрофии, фиброзирования, а также различных интоксикаций (в т.ч. некоторыми лекарственными препаратами: сердечными гликозидами, р-адреноблокаторами). По ЭКГ-признакам СССУ является полиморфной формой нарушения электрической функции сердца. Прежде всего, синдром рассматривают в качестве достаточно частой причины брадикардии. СССУ может также проявляться преходящей синоатриальной блокадой (нарушением проведения электрического импульса из синусового узла к предсердиям) и «синус-арестом» (прекращением автоматической активности синусового узла).
При брадикардии, обусловленной СА-блокадой, интервал Р-Р во время паузы, как правило, кратен основному интервалу Р-Р, в то время как при остановке синусового узла такая связь не наблюдается. Кроме того, при СССУ возможно развитие т.н. синдрома «брадикардия-тахикардия», т.е. чередование периодов выраженной брадикардии и тахикардии. При значительном снижении автоматизма синусового узла создаются условия для периодического проявления центров автоматизма II и III порядка. При этом возникают различные несинусовые эктопические ритмы (чаще предсердные, из АВ-соединения, мерцание и трепетание предсердий и т. д.).
В условиях развития стойкой синусовой брадикардии рекомендуется проводить пробу с атропином. После регистрации исходной ЭКГ подкожно вводится 1 мл 0,1 % раствора атропина, контрольные ЭКГ через 30 минут и через час. При функциональной форме брадикардии происходит учащение ритма (более 90 в 1 минуту); отсутствие такого эффекта – признак органического поражения синусового узла.
Хотя синусовые паузы и остановки синусового узла могут не иметь существенного клинического значения, появление замещающих предсердных или узловых водителей ритма для предотвращения асистолии желудочков повышает риск фибрилляции и трепетания предсердий и, как следствие, тромбоэмболических осложнений — тромбоэмболии легочных артерий, ишемического инсульта или инфаркта миокарда.
Синдром брадикардии-тахикардии обычно ассоциируется с клиническими проявлениями, тис слишком частое подавление автоматизма синусового узла во время эпизодов тахикардии может приводить к длительным паузам вследствие увеличения времени его восстановления.
Синдром Морганьи—Адамса—Стокса
Синдром Морганьи—Адамса—Стокса, Одной из наиболее серьезных и опасных форм синдрома слабости синусового узла является синоаурикулярная блокада. Если возникающая при этом асистолия желудочков затягивается, развиваются выраженнные гемодинамические нарушения, приводящие, прежде всего, к гипоксии головного мозга. У больного нарушается высшая нервная деятельность, происходит потеря сознания, развиваются приступы судорог и, в завершение — бульбарные расстройства, которые могут приводить к летальному исходу.
Во время приступа пульс не пальпируется, тоны сердца не выслушиваются, артериальное давление не определяется, лицо вначале бледное, а затем постепенно становится цианотичным; развивается диспноэ, сменяющееся претерминальным апноэ и гаспинг-дыханием Такие приступы, получившие название синдром/приступ Морганьи—Адамса—Стокса, зачастую прекращаются самостоятельно или благодаря проведению соответствующих реанимационных мероприятий.