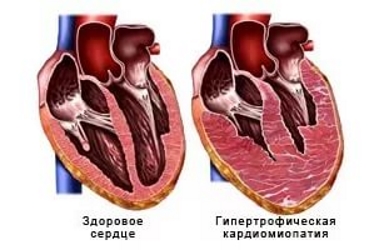
Гипертрофическая кардиомиопатия: понятие, виды, причины
Содержание
Что такое гипертрофическая кардиомиопатия
Гипертрофическая кардиомиопатия — это весьма редкое наследственное, т.е. первичное по происхождению заболевание, характеризующееся гипертрофией левого желудочка при отсутствии каких-либо признаков врожденных и приобретенных пороков сердца, системной артериальной гипертензии и других форм патологии, способных вызывать его гипертрофию.
Расстройство имеет переменную картину и имеет высокую частоту внезапной смерти. На самом деле, гипертрофическая кардиомиопатия (ГКМ) является основной причиной внезапной сердечной смерти у детей до и подросткового возраста. Отличительной чертой этого расстройства является гипертрофия миокарда, которая часто асимметрична и возникает при отсутствии явного стимула гипертрофии. Эта гипертрофия может возникать в любой области левого желудочка, но часто включает межжелудочковую перегородку, что приводит к обструкции потока через левый желудочек тракта оттока.
У многих больных, особенно детей, с ГКМ может не иметься симптомов. Тщательная оценка шумов в сердце может выявить заболевание.
Виды
Гипертрофическую кардиомиопатию классифицируют по ее анатомическому паттерну, наблюдаемому в левом желудочке. Наиболее часто (примерно в 90% случаев) гипертрофия является асимметричной и относится к желудочковой перегородке. При гистологическом исследовании в ней обнаруживают беспорядочно расположенные кардиомиоциты, образующие хаотическую, а не обычную упорядоченную, характерную для нормального миокарда структурированную ткань с параллельно расположенными миоцитами. При этом в некоторых гипертрофированных кардиомиоцитах выявляют дистрофические изменения, вплоть до необратимой альтерации с развитием заместительного склероза. Кроме того, постоянным патогистологическим признаком гипертрофической кардиомиопатии является увеличение содержания в миокарде соединительной ткани вследствие интерстициального фиброза и в меньшей степени заместительного склероза.
Функционально гипертрофическую кардиомиопатию чаще всего классифицируют по механизму обструкции пути оттока крови из левого желудочка.
Примерно у четверти больных гипертрофической кардиомиопатией гипертрофия перегородки является причиной обструкции пути оттока крови из левого желудочка во время систолы.
Во время диастолы желудочек заполняется через открытое митральное отверстие. При этом из-за утолщения (гипертрофии) и фиброзирования стенки желудочка процесс его заполнения (обозначен волнистой стрелкой) затрудняется. В ранний период систолы (период выброса начальной порции крови из левого желудочка) поток крови проходит через открытый аортальный клапан аномально близко (опять же из-за утолщенной стенки) к митральному отверстию.
В середине систолы утолщенная перегородка, суживающая выходной путь кровотоку, детерминирует эффект Вентури (ГУ): перетягивание передней створки митрального клапана к перегородке (митральная створка может даже к ней прикоснуться), что вызывает динамическую обструкцию аортального отверстия. При этом сердечный выброс существенно уменьшается, несмотря на значительное увеличение внутрижелудочкового давления. Описанное препятствие выбросу крови является патогенетически значимым преимущественно в середине или конце систолы, т.е. в моменты наибольшей постнагрузки на желудочек.
В условиях, когда гипертрофированное сердце подвергается внезапному увеличению постнагрузки, кривая диастолического давления смещается вверх и принимает более крутой угол подъема, а кривая иэоволюмического систолического давления перемещается лишь немного вверх по сравнению с аналогичной кривой в норме.
При этом ударный объем уменьшается, несмотря на заметное повышение конечного диастолического давления. Патогенетической основой всех этих изменений является уменьшение комплаенса и растяжимости гипертрофированного сердца.
Причины
Методы молекулярной биологии значительно расширили представление о гипертрофической кардиомиопатии. Установлено, что это гетерогенная форма патологии, которая наследуется по аутосомно-доминантному типу.
На сегодняшний день выявлены хромосомы (это 1,11,14 и 15 хромосомы), мутации в которых детерминируют данную форму патологии. Ген (J-MHC (главного комплекса тканевой совместимости) существует на хромосоме 14. Белок р-МНС является основным компонентом для толстых нитей саркомера у взрослых. К настоящему времени идентифицировано более 36 различных мутаций этого гена. Аномальные белки миозина образуют дефектные саркомеры. По статистике мутации гена р-МНС составляют в основном 20—40% случаев гипертрофической кардиомиопатии.
Мутации гена тропонина-Т (расположен в хромосоме 1) и гена тропомиозина (расположен в хромосоме 15) детерминируют другие варианты данной формы патологии. Очевидно, все такие патогенные мутации (известные и пока еще не выявленные) вызывают аномальные изменения микроархитектуры и функции саркомеров. В подавляющем большинстве случаев развития гипертрофической кардиомиопатии не выявлено какое-либо ее защити о-приспособительное значение для организма. В том числе, это относится и к рассмотренной здесь септальной форме гипертрофии левого желудочка.
Установлено, что ~ у 10—15% пациентов с длительной гипертрофической миокардиопатией со временем развивается систолическая дисфункция. У таких больных стенки левого желудочка истончаются (не всегда! и могут сохранять свою толщину), в них происходит диффузное разрастание соединительной ткани, объем его полости увеличивается. Данная форма патологии получила название “дилатационная кардиомиопатия”.
Аномальная кинетика кальция
Данные связывают аномальную кинетику кальция в миокарде с причиной неадекватной гипертрофии миокарда и специфических особенностей ГКМ, особенно у пациентов с диастолическими функциональными нарушениями. Ненормальная кинетика кальция в миокарде и аномальные потоки кальция из-за увеличения количества кальциевых каналов приводят к увеличению внутриклеточной концентрации кальция, что, в свою очередь, может привести к гипертрофии и нарушению работы клеток.
Генетические причины
ГКМ встречается как аутосомно-доминантное заболевание, унаследованное по Менделю, примерно в 50% случаев. Некоторые, если не все, спорадические формы заболевания могут быть вызваны спонтанными мутациями.
По крайней мере, 6 различных генов, по крайней мере, в 4 хромосомах связаны с ГКМ, с более чем 50 различными мутациями, обнаруженными к настоящему времени. Семейная ГКМ является генетически гетерогенным заболеванием, которое может быть вызвано генетическими дефектами в более чем 1 локусе.
Другие возможные причины
Другие возможные причины ГКМ включают в себя следующее:
-
Ненормальная симпатическая стимуляция – повышенная чувствительность сердца к чрезмерной выработке катехоламинов или уменьшенному поглощению нейронами норадреналина может вызвать ГКМ
-
Аномально утолщенные интрамуральные коронарные артерии – они обычно не расширяются, что приводит к ишемии миокарда; это прогрессирует до фиброза миокарда и патологической компенсаторной гипертрофии
-
Субендокардиальная ишемия – это связано с нарушениями микроциркуляции в сердце, которые истощают запасы энергии, необходимые для секвестрации кальция во время диастолы; субэндокардиальная ишемия приводит к постоянному взаимодействию сократительных элементов во время диастолы и увеличению диастолической жесткости
-
Структурные аномалии сердца – к катеноидной конфигурации перегородки, что приводит к гипертрофии и разрушению клеток миокарда
Патофизиология
Начиная с начальных описаний гипертрофической кардиомиопатии, особенность, которая привлекла наибольшее внимание, – это динамический градиент давления через тракт оттока левого желудочка. Градиент давления, по-видимому, связан с дальнейшим сужением и без того маленького тракта оттока (уже суженного заметной асимметричной септальной гипертрофией и, возможно, аномальным расположением митрального клапана) систолическим передним движением митрального клапана против гипертрофированной перегородки.
Предлагалось три объяснения систолического переднего движения митрального клапана, а именно:
1) митральный клапан притягивается к перегородке за счет сокращения папиллярных мышц, что происходит из-за неправильного расположения клапана и гипертрофии перегородки, изменяющей ориентацию папиллярных мышц;
2) митральный клапан прижимается к перегородке из-за его ненормального положения в пути оттока;
3) митральный клапан притягивается к перегородке из-за более низкого давления, которое возникает, когда кровь выбрасывается с высокой скоростью через суженный тракт оттока (эффект Вентури).
У большинства лиц с ГКМ имеется аномальную диастолическую функцию (присутствует или нет градиент давления), что ухудшает наполнение желудочков и увеличивает давление наполнения, несмотря на нормальную или небольшую желудочковую полость. У этих больных имеется аномальная кинетика кальция и субэндокардиальная ишемию, которые связаны с глубокой гипертрофией и миопатическим процессом.
Лечение
Диагностика обычно может проводиться амбулаторно. Стационарные исследования и хирургическое лечение также могут быть необходимы. Медицинская и хирургическая терапия используются для уменьшения сократимости желудочков или увеличения объема желудочков, увеличения податливости желудочков и размеров путей оттока, а в случае обструктивной гипертрофической кардиомиопатии, снижения градиента давления в тракте оттока левого желудочка. Первостепенное значение для любой терапии имеет понижение риска внезапной смерти путем раннего выявления этих пациентов и эффективной медицинской и / или хирургической имплантации автоматического дефибриллятора.
Медикаменты включают бета-блокаторы, блокаторы кальциевых каналов и, редко, дилтиазем, амиодарон и дизопирамид. Противокашлевые средства могут применяться по мере необходимости, чтобы избежать кашля.
Клинические исследования показывают, что ступенчатая терапия может снизить высокое кровяное давление у пациентов с ГКМ.
Следует по-возможности избегать прима инотропных препаратов. Также следует избегать нитратов и симпатомиметических аминов, за исключением для лиц с сопутствующим заболеванием коронарной артерии. Следует осторожно использовать диуретики из-за их потенциального вредного влияния на градиент оттока левого желудочка и объем желудочков.